El proyecto fue llevado a cabo por un equipo de investigadores de la Universidad de Ohio, que incluyó a dos destacados científicos chilenos: la profesora Verónica Bahamondes, tecnóloga médica, doctora en Química y Bioquímica, y académica del Departamento de Tecnología Médica de nuestra facultad, quien actualmente se desempeña como investigadora en Ohio; y el doctor Óscar Ávalos, doctor en Física, quien está realizando su postdoctorado en la misma institución.
¿Qué es un test rápido?
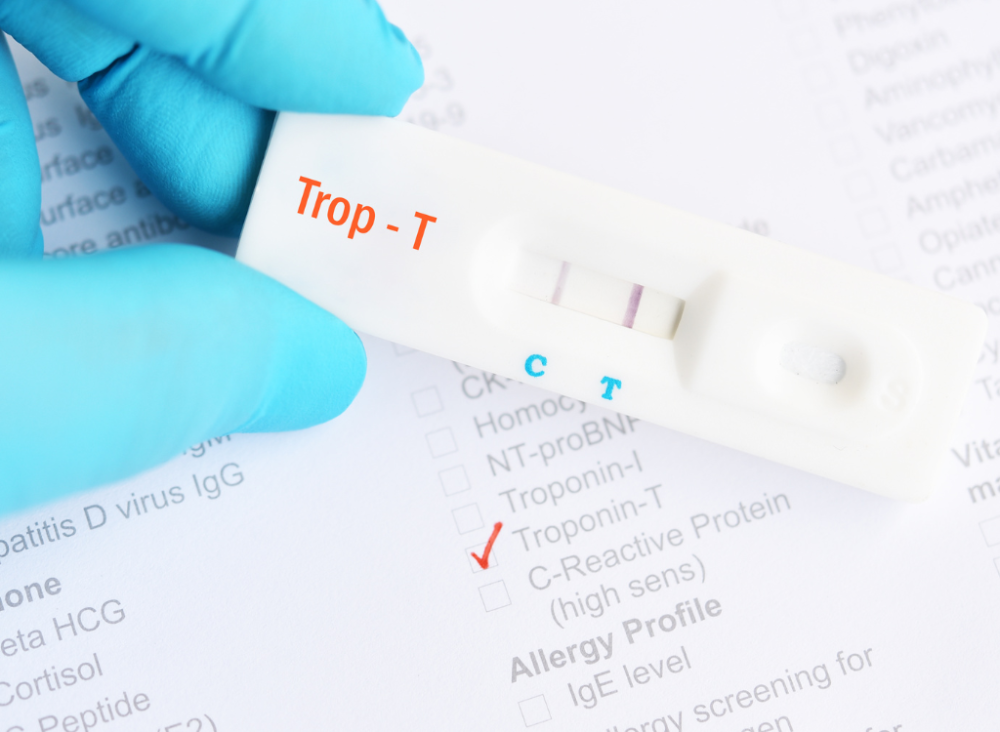
Las pruebas biológicas de flujo lateral LFA (por sus siglas en inglés “Lateral Flow Assays”), también conocidas como test de detección rápida o test de papel, son “una herramienta diagnóstica que vimos bastante durante el periodo de COVID-19. Son tiras de papel especial que contienen un sistema de anticuerpos capaces de detectar proteínas de interés”, explicó la profesora Verónica Bahamondes. “Por ejemplo, en el caso del COVID-19, estos análisis detectaban una proteína que indicaba la presencia del virus”, añadió.
El mecanismo de acción de estas pruebas “se basa en un principio bastante simple, pero poderoso”, afirmó la académica. “Los test rápidos funcionan por difusión simple, y se componen de cuatro elementos fundamentales”.
El primero corresponde a “un sistema de captura de proteínas, compuesto por anticuerpos que están localizados de forma fija en la tira de papel, justamente donde se marcan las dos rayas que indican que el examen es positivo, tal como ocurre en los conocidos test de embarazo”, comenzó explicando la profesora Bahamondes.
El segundo y tercer componente corresponden a nanopartículas de oro y anticuerpos libres: “Estas nanopartículas de oro se unen previamente, a través de un proceso de sintetización química, a anticuerpos libres. Estos dos componentes, en conjunto, forman las llamadas partículas de detección, las cuales son capaces de reconocer de forma específica la proteína de interés”, detalló la académica.
En otras palabras, además de los anticuerpos fijos situados en la zona de captura, “en la tira de papel existen anticuerpos libres que están conjugados con una nanopartícula de oro, y que al momento de mezclarse con la muestra, se unen a la proteína de interés, y se desplazan por difusión simple hasta llegar a la zona de captura”, agregó.
El cuarto y último elemento del examen “es justamente la muestra proporcionada por el paciente, que se aplica directamente sobre el papel. Esta muestra puede ser, por ejemplo, orina —como en el caso de los test de embarazo—, saliva, sangre, entre otras”, continuó la profesora.
Al momento de realizar el análisis, se presume que la muestra contiene la proteína que se desea detectar: “Si efectivamente está presente, se unirá a las partículas de detección —formadas por nanopartículas de oro conjugadas con anticuerpos libres—, y se desplazará por difusión simple hasta unirse al sistema de captura. Esta unión indicará una reacción positiva con la coloración de dos rayitas”, explicó la doctora Verónica Bahamondes.
Dicha coloración, que se observa en forma de dos rayas rojizas que aparecen en la tira de papel, ocurre gracias a las nanopartículas de oro: “Cuando se produce el encuentro entre el complejo anticuerpo-oro-proteína, y el sistema de captura, se forma lo que nosotros llamamos un «sándwich», integrado por los cuatro componentes: sistema de captura, anticuerpos libres unidos a nanopartículas de oro, y las proteínas de interés”, explicó la académica. “Lo que permite que este sándwich se torne de color rojizo, son las nanopartículas de oro, que al momento del contacto reaccionan químicamente, permitiéndonos observar el resultado”, añadió.
Cobre y nitruro de titanio como alternativas al oro
Los test rápidos son capaces de detectar diferentes tipos de proteínas. Uno de los más conocidos y utilizados es la prueba de embarazo, que cumple con todos los principios descritos anteriormente. “Estos exámenes sirven para detectar cualquier patología o condición que cause un aumento en alguna proteína o molécula, que sea viable de ser reconocida por anticuerpos”, explicó la profesora Verónica Bahamondes.
Pero, a pesar de las numerosas ventajas que ofrece este sencillo dispositivo, su distribución masiva se ve sumamente limitada: “El elevado costo del oro, necesario para la fabricación de los test, así como la complejidad que se requiere para sintetizar las nanopartículas de oro-anticuerpo, actualmente impiden que contemos con mayor variedad en el mercado. Si los costos de producción y distribución fueran menores, las LFA podrían ser fácilmente utilizadas por las personas en sus casas, para detectar diabetes o infartos, por ejemplo”, afirmó la profesora Verónica Bahamondes.
Además, “si uno piensa en el futuro, la abundancia y biodisponibilidad del oro podría verse comprometida. Si eso sucede, nos quedaríamos sin esta herramienta, que es tan útil en la actualidad”, agregó.
La académica del Departamento de Tecnología Médica comentó que “durante bastante tiempo, sobre todo debido a la emergencia sanitaria del COVID-19, se potenció la búsqueda de métodos para mejorar la sensibilidad del test. Pero nadie se detuvo a pensar en formas de rebajar los costos, ni en buscar alternativas al uso del oro. Y justamente eso fue lo que hicimos nosotros: buscar reemplazos, otras opciones que fueran igual de efectivas, para sustituir las nanopartículas de oro”.
Para realizar esto, los investigadores de Ohio, junto con la profesora Bahamondes, decidieron trabajar con la detección de troponina: “La troponina es una proteína que se libera a la sangre cuando el músculo cardiaco sufre daños debido a un infarto agudo al miocardio. El nivel de troponina en la sangre puede ser detectado mediante un test rápido”, indicó nuestra académica.
En este caso, las pruebas de detección de troponina se realizaron “utilizando los nuevos test que desarrollamos, en los que reemplazamos las nanopartículas de oro por cobre recubierto con una fina capa de oro, o por partículas de nitruro de titanio”, explicó.
En el caso de las nanopartículas de cobre, “seguimos utilizando una fina capa de oro para recubrirlo, debido a que este mineral suele oxidarse o precipitar fácilmente. Pero a pesar de seguir utilizando oro como recubrimiento, el costo de producción es sustancialmente menor al de las partículas clásicas”, afirmó la doctora.
En cuanto a la eficacia, estas nuevas partículas de detección “demostraron ser igual de efectivas que las partículas de oro tradicionales, y tal como en los test rápidos clásicos, la coloración se produce en un tono rojizo”, aseveró la profesora Bahamondes.
Por otra parte, se trabajó con nanopartículas hechas de nitruro de titanio, las cuales presentaron los resultados más prometedores: “El nitruro de titanio mostró ser sumamente estable durante los testeos, funcionando incluso mejor que las partículas de oro”, sostuvo la profesora Verónica Bahamondes. “Además, es fácil de sintetizar y su costo de producción es hasta 10.000 veces menor a los de las partículas clásicas”, añadió. “La única diferencia es que la coloración de las rayas en el papel se visualiza de color negro”, concluyó.
Las futuras aplicaciones
La búsqueda de nuevas alternativas a los test rápidos usados en la actualidad surgió a partir de una necesidad: “En el caso de los ataques cardiacos, por ejemplo, muchas veces los pacientes sienten dolor, pero no acuden de inmediato a un centro de urgencias. De ahí la utilidad e importancia de que este tipo de exámenes puedan ser realizados de forma fácil y económica en casa”, declaró la profesora Verónica Bahamondes.
Con esto en mente, “un grupo de investigadores de Ohio comenzó a indagar en opciones para mejorar la eficiencia de las LFA, o encontrar una manera de reducir costos”, añadió.
Fue entonces cuando el trabajo tomó forma: “El profesor Óscar Ávalos, quien trabaja en un grupo de física teórica, fue quien realizó simulaciones para evaluar la visibilidad de las nanopartículas al ojo humano, y la eficiencia de su uso según su comportamiento”, detalló la profesora.
Así se llegó a la decisión de utilizar cobre y nitruro de titanio como materiales principales: “Las simulaciones teóricas mostraron que estas dos nanopartículas eran fácilmente visibles a simple vista, lo que las hacía adecuadas para su aplicación en una LFA”, señaló. “En esa fase comenzó mi trabajo, enfocado en el desarrollo experimental y bioquímico de la síntesis de partículas”, mencionó.
La profesora Verónica Bahamondes destacó que el desarrollo de los nuevos test fue un esfuerzo colaborativo entre varias organizaciones: “La estandarización de las partículas se realizó en conjunto con grupos de investigación de Alemania, mientras que la síntesis de cobre con oro provino de Canadá, y las de nitruro de titanio fueron desarrolladas en Francia”, explicó. “La conjugación final de las partículas y los test se llevó a cabo aquí en Ohio”, subrayó.
La investigación comenzó el 2022, y “considerando la obtención de resultados y publicación del trabajo final, el proceso tomó alrededor de un año y medio”, señaló la doctora Verónica Bahamondes. Además, anticipó que el desarrollo seguirá avanzando: “Actualmente, estamos trabajando con nuevas nanopartículas de cobre desarrolladas por un laboratorio en Canadá, que son mucho más resistentes y estables, por lo que no requieren de oro para protegerlas de la oxidación o precipitación”, expuso la profesora Bahamondes.
Con miras al futuro próximo, “esperamos que los test desarrollados con nitruro de titanio, que demostraron ser los más eficientes, puedan ser probados en otros sistemas, como por ejemplo, en la detección de diabetes o embarazo. La idea es ofrecer una alternativa más accesible y económica a los test actuales, que pueda distribuirse de forma masiva y demostrar a la comunidad científica que estas partículas pueden ser efectivamente utilizadas para desarrollar este tipo de tecnologías”, aseveró.
Además, “estas partículas tienen la capacidad de generar bastante calor debido a sus propiedades plasmónicas, hecho que las hace posiblemente aplicables a otras tecnologías, como por ejemplo, en la terapia a través de calor. Aunque aún estamos lejos de llegar a eso, es una posibilidad real”, concluyó la profesora.
Actualmente, estos nuevos test de detección rápida se encuentran en proceso de patente a través de la Universidad de Ohio. El trabajo final, liderado por el doctor Alexander Govorov, profesor de dicha institución, se encuentra publicado y disponible para su revisión en la revista científica Nano Letters.